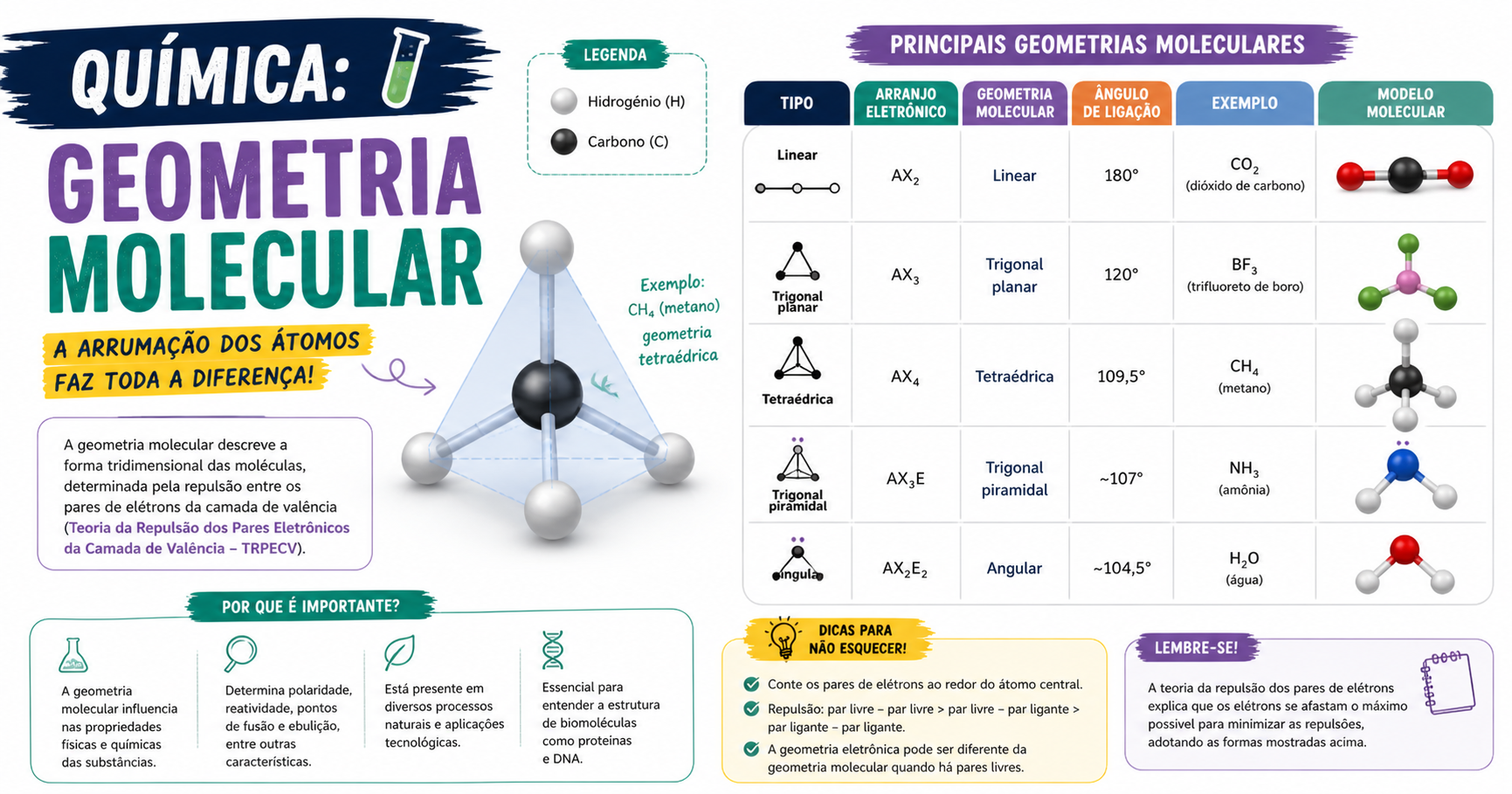
Geometria Molecular: entenda a forma das moléculas
A geometria molecular é o estudo da forma tridimensional das moléculas, ou seja, da maneira como os átomos se organizam no espaço.
Esse conteúdo é muito importante na Química porque a forma de uma molécula influencia diretamente suas propriedades, como polaridade, solubilidade, ponto de ebulição e reatividade química.
O que é geometria molecular?
A geometria molecular descreve a disposição espacial dos átomos em uma molécula. Essa organização depende principalmente da quantidade de átomos ligados ao átomo central e da presença de pares de elétrons livres.
Para explicar essas formas, usamos a Teoria da Repulsão dos Pares Eletrônicos da Camada de Valência (TRPECV).
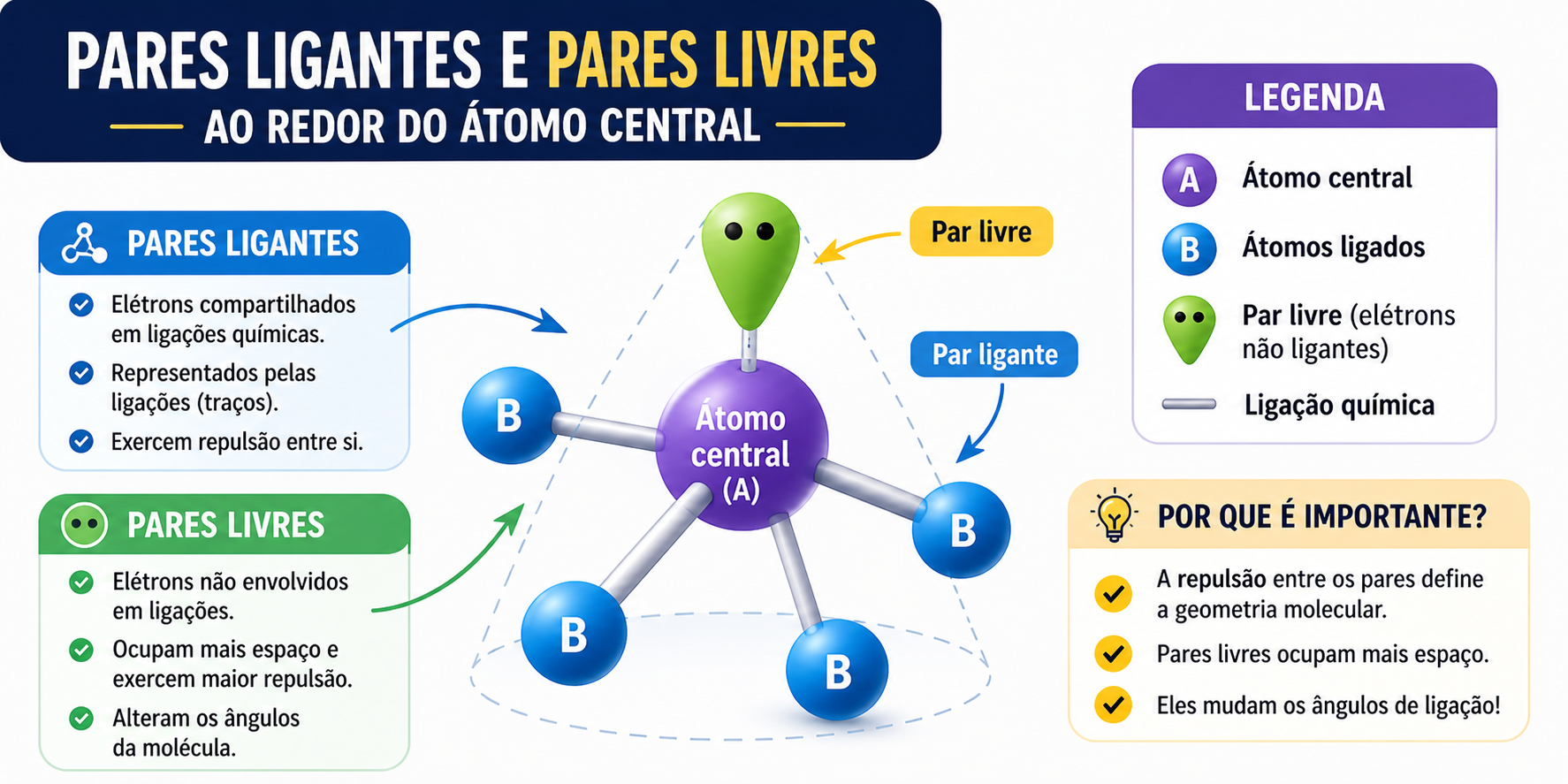
Pares ligantes e pares livres ao redor do átomo central.
Por que as moléculas possuem formatos diferentes?
Os pares de elétrons ao redor do átomo central se repelem, pois possuem carga negativa. Por isso, eles tendem a se afastar o máximo possível uns dos outros, formando diferentes geometrias.
- Pares ligantes: participam das ligações químicas;
- Pares livres: não participam das ligações e causam maior repulsão.
Principais geometrias moleculares
1. Geometria linear
A geometria linear ocorre quando os átomos ficam organizados em linha reta, formando ângulo de aproximadamente 180°.
Um exemplo clássico é o CO2, o dióxido de carbono.
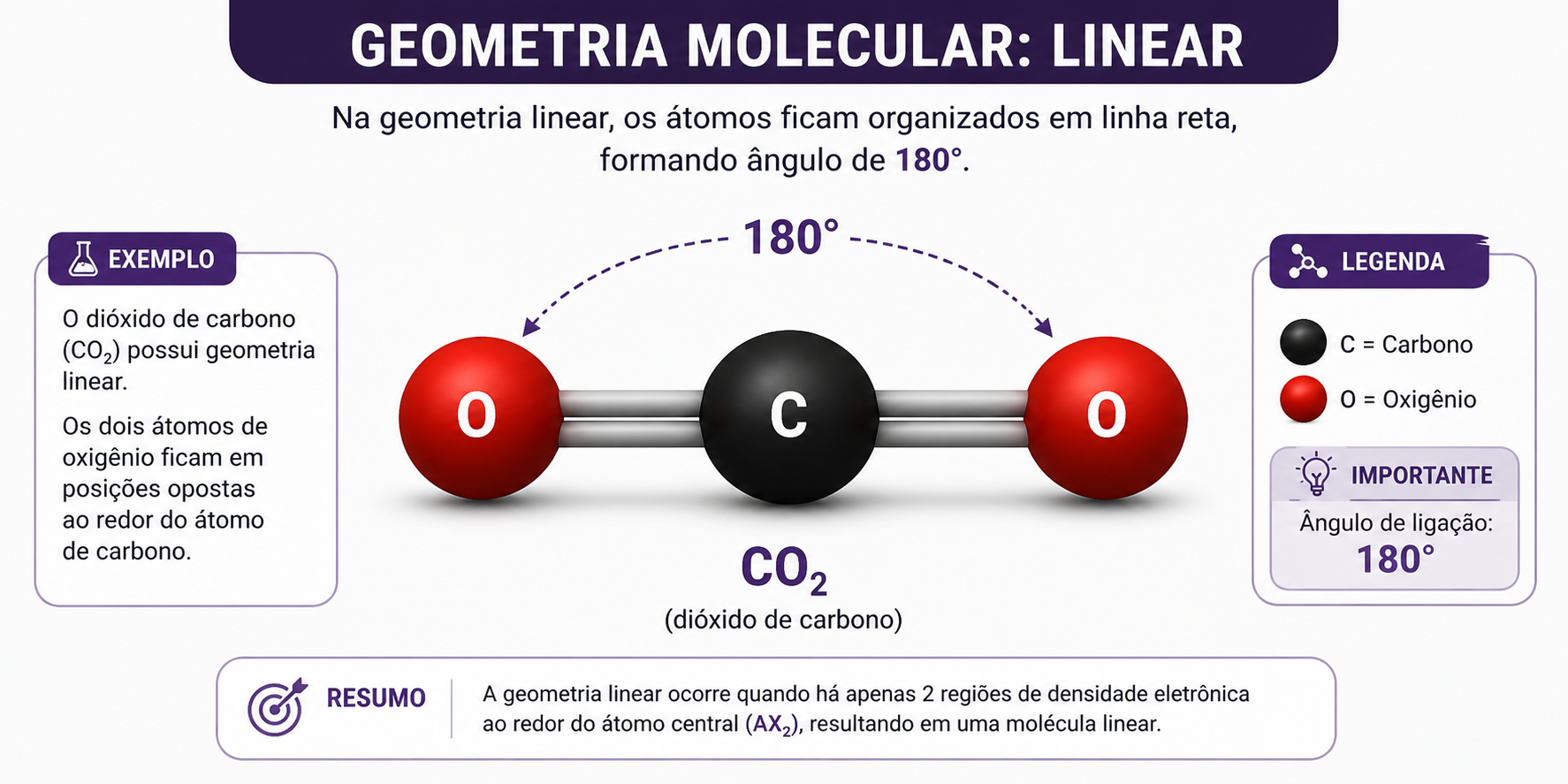
Estrutura linear do dióxido de carbono (CO₂), com ângulo de 180°.
2. Geometria trigonal plana
Três átomos organizados no mesmo plano, formando ângulos de aproximadamente 120°. Exemplo: BF3.
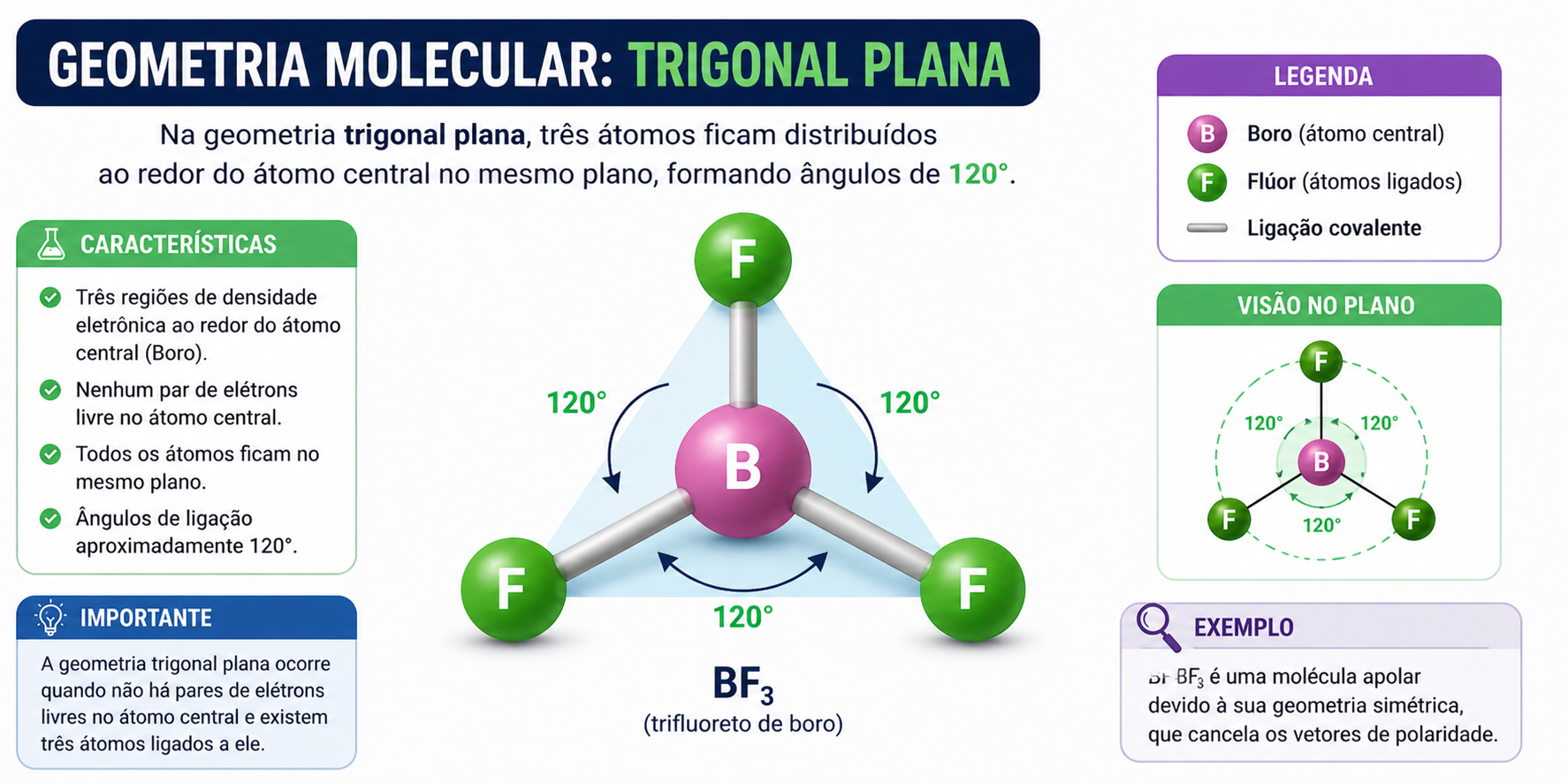
Molécula trigonal plana do BF3.
3. Geometria tetraédrica
Quatro átomos ao redor do átomo central, formando ângulos de 109,5°. Exemplo: CH4.
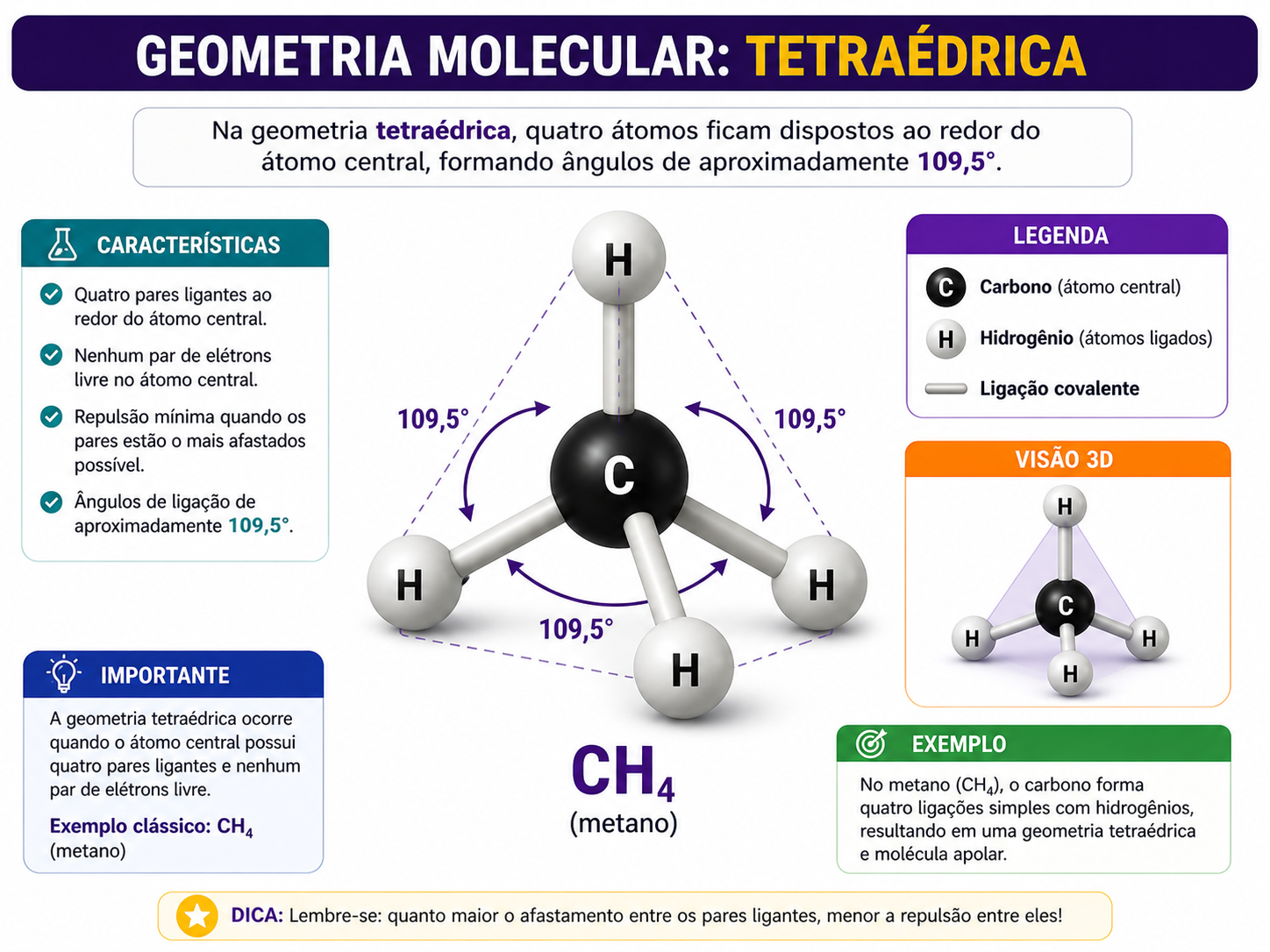
Molécula tetraédrica do CH4.
4. Geometria trigonal piramidal
Três átomos ligados e um par de elétrons livre. Exemplo: NH3.
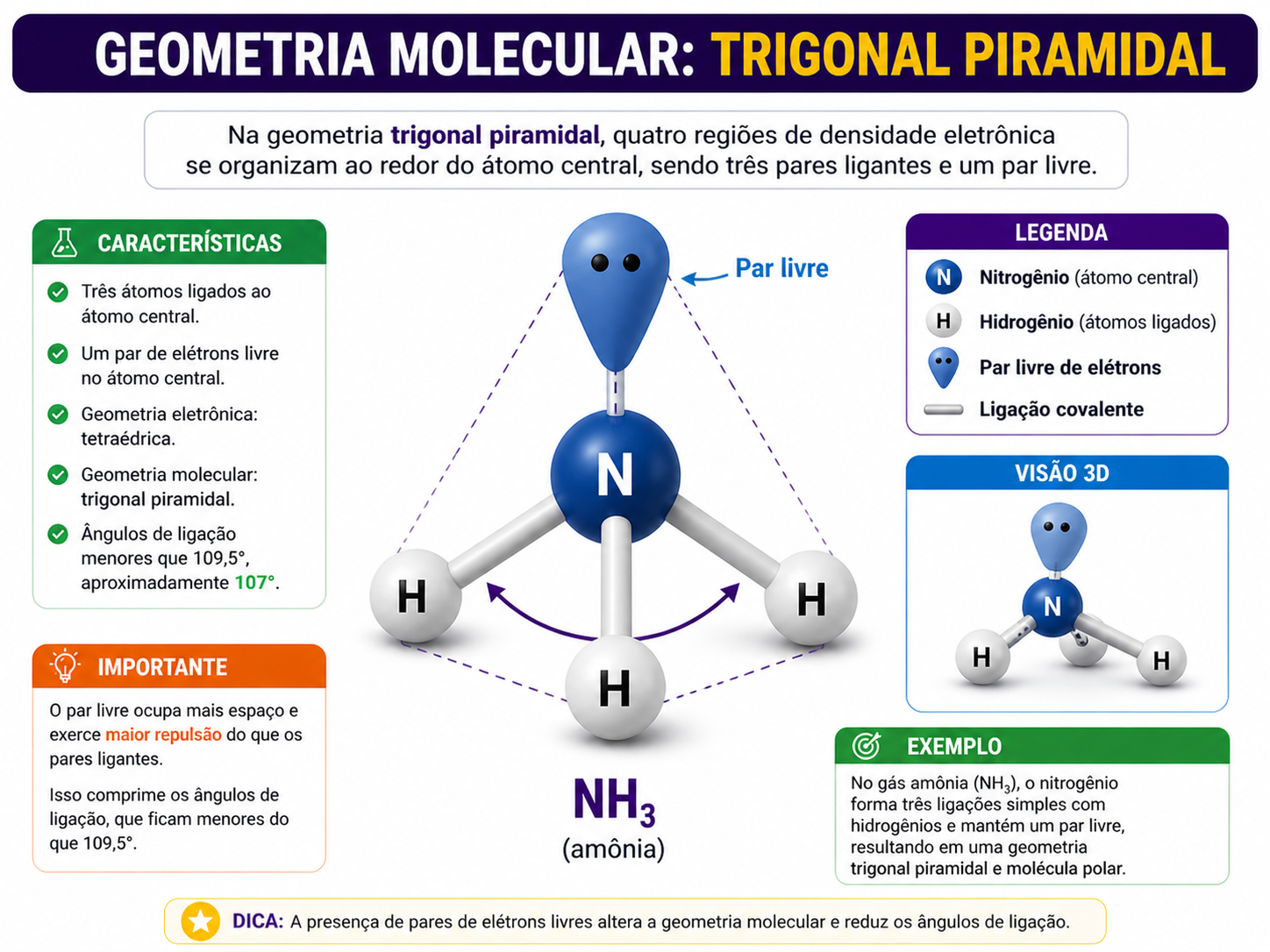
Molécula trigonal piramidal da NH3.
5. Geometria angular
Dois átomos ligados e pares livres alterando a forma. Exemplo: H2O.
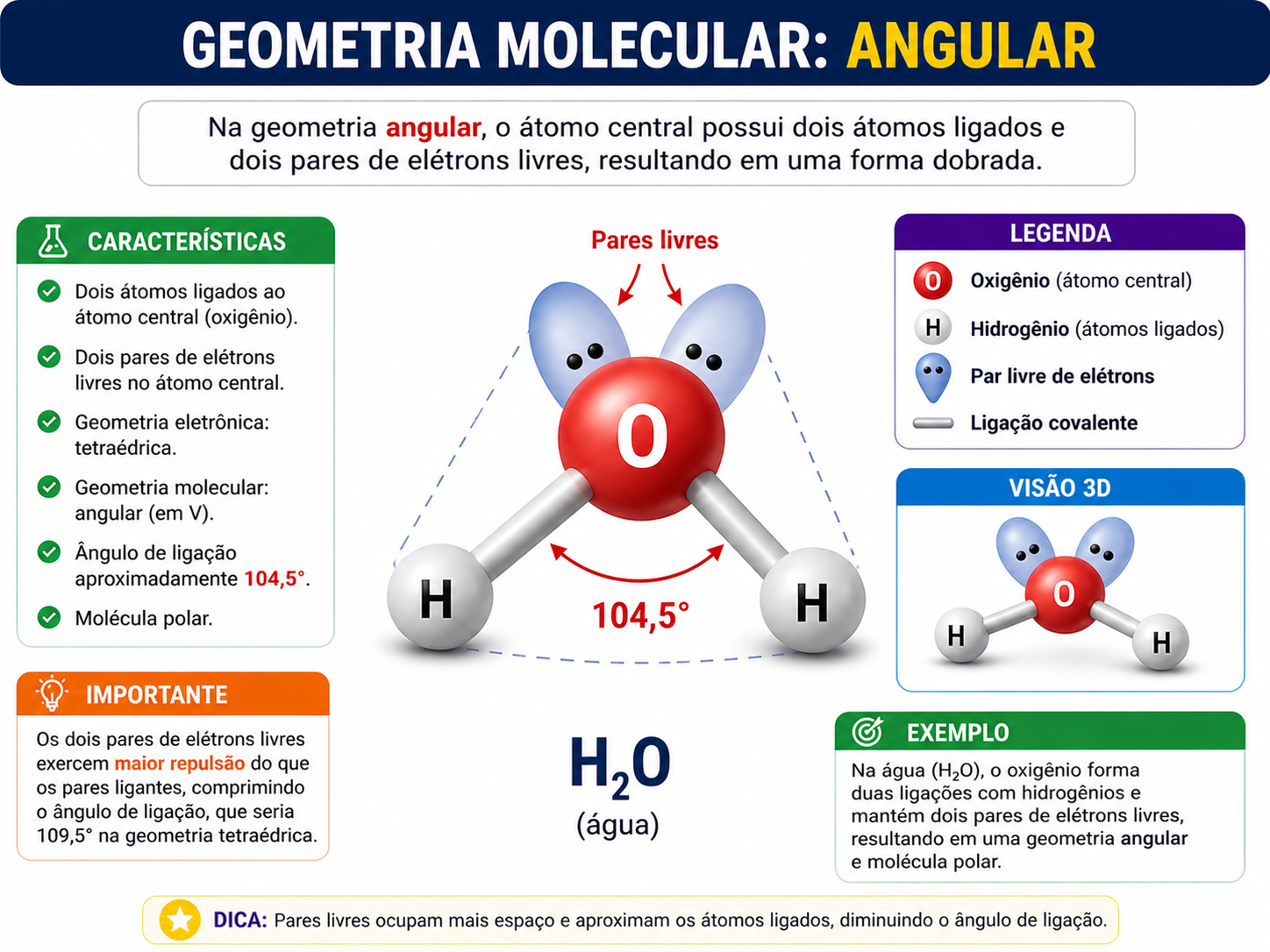
Molécula angular da água.
Geometria molecular e polaridade
A geometria molecular ajuda a determinar se uma molécula é polar ou apolar.
Mesmo com ligações polares, uma molécula pode ser apolar se houver cancelamento dos vetores de dipolo, como no CO2.
Já moléculas com geometria angular, como a água, são polares.
Como identificar a geometria molecular?
- Identifique o átomo central;
- Conte os átomos ligados a ele;
- Verifique pares de elétrons livres;
- Analise a repulsão eletrônica;
- Determine a geometria.
Resumo
A geometria molecular é essencial para entender o comportamento das substâncias. Quanto mais você visualizar as estruturas, mais fácil será interpretar questões do ENEM.